Midiendo la Dosis de Hemodiálisis
En medicina, una “dosis” se refiere a la cantidad de un medicamento en particular que toma un paciente. Sin embargo, en diálisis la “dosis” se mide por el efecto producido por una determinada prescripción. Más específicamente, se refiere a la cantidad de un marcador tóxico particular que se elimina de la sangre de un paciente. La urea y la creatinina son los marcadores más utilizados para medir la idoneidad de la dosis de diálisis1. Se miden como marcadores sustitutos de la eficacia de un tratamiento de diálisis para limpiar la sangre de toxinas y productos finales metabólicos. Al eliminar una cantidad adecuada de este marcador (es decir, lograr una dosis de diálisis adecuada), es posible reducir la morbilidad y la mortalidad, controlar los síntomas y mejorar la calidad de vida2.
Se han propuesto muchos métodos para medir la dosis de diálisis; sin embargo, la más utilizada es la urea Kt/V. La urea es un pequeño compuesto soluble en agua que se forma a partir de la descomposición de aminoácidos y depende de la ingesta y descomposición de proteínas. Muchos de los primeros estudios implicaron a la urea como una de las principales toxinas corporales3 y originalmente se consideró que era un buen marcador sustituto de otros solutos patógenos4. La urea se utiliza actualmente para cuantificar la dosis de diálisis por su abundancia en insuficiencia renal, facilidad de medición, amplio volumen de distribución y buena dializabilidad1,5,6.
El concepto detrás de la urea Kt/V surgió de un nuevo análisis del National Cooperative Dialysis Study (NCDS) realizado por Gotch y Sargent en 19857. Los investigadores demostraron que los resultados clínicos podrían predecirse mejor cuando la dosis de diálisis se expresó como el producto de urea del dializador. aclaramiento (K) y tiempo de tratamiento (t), dividido por el volumen de distribución de urea (V)3,7–9. El resultado fue un número inexpresivo que describía el volumen de urea eliminado durante una sesión de diálisis en relación con el volumen de urea distribuido por todo el cuerpo4 (ver más abajo).
(K (mL/min) × t (min))/V(mL)
Suponiendo que no hay ultrafiltración o generación de urea, la urea Kt/V administrada se puede calcular a partir de la concentración de urea al inicio y al final de la diálisis utilizando la fórmula siguiente1. En la ecuación, ln representa el logaritmo natural, Co es la concentración de urea inicial y Ct es la concentración de urea final.
Kt/V = ln(C0/Ct )
Desafortunadamente, una ecuación tan simple no puede explicar otros factores que pueden afectar la dosis administrada de diálisis1,10. La concentración final de urea no solo depende de la eliminación de urea por el dializador, sino también de la generación de urea (G) y los efectos convectivos de la ultrafiltración. De manera similar, el volumen de distribución de la urea (V) no es fijo y variará según la eliminación del agua intradialítica. Como tal, el modelado cinético de urea (UKM) (a veces llamado UKM formal) se desarrolló como un método más preciso para determinar Kt/V1,3,10-12. Estos modelos simulan el movimiento de la urea durante la sesión de diálisis y derivan los valores de V y G para calcular la dosis de diálisis1,11,12 (ver Tabla 1). Por lo tanto, estas ecuaciones pueden explicar los efectos de confusión de la ultrafiltración y la generación de urea10,12.
Tabla 1
| Variables Estimadas Usando Modelamiento de Urea Quinetica (UKM) | |
| Variable | Explicación |
| V | Volume de distribucion de urea, que equipara cerca al agua corporal |
| G | Generación de urea en diálisis |
| PCRn | Tasa catabólica de proteínas normalizada, que se estima a partir de G; en pacientes estables, PCRn es igual a proteína dietética |
| K | Aclaramiento del dializador extrapolado del coeficiente de área de transferencia de masa del dializador (KoA) |
| Tabla adaptada de referencia11 | |
UKM es actualmente el método preferido para determinar Kt/V por las Directrices KDOQI de la National Kidney Foundation5 y se utilizó en el reanálisis de NCDS discutido anteriormente7. Se han desarrollado varios UKM diferentes para cuantificar Kt/V, incluido el Kt/V de grupo único, Kt/V equilibrado y Kt/V estándar semanal.
Grupo único Kt/V (spKt/V)
El modelo más común para calcular Kt/V se basa en el supuesto de que la urea se encuentra en un solo compartimento (o grupo) del cuerpo4,10,13. Esta idea de un grupo único de Kt/V (spK/V) predice una disminución lineal de la urea y un equilibrio inmediato entre los compartimentos de sangre y tejido después de la diálisis. Por tanto, el spKt /V se calcula midiendo la concentración de BUN previa a la diálisis, seguida de la concentración de BUN posterior a la diálisis 10-15 segundos después del final de la diálisis5,8. El tiempo de retraso se utiliza para explicar los efectos de confusión de la recirculación de sangre dentro de la fístula8,12. Las pautas actuales de KDOQI sobre la adecuación de la hemodiálisis recomiendan que la dosis mínima adecuada para el tratamiento convencional, tres veces por semana, sea un spKt/V de 1,2, con una dosis objetivo de 1,45.
La siguiente ecuación es un ejemplo de una fórmula UKM logarítmica simplificada de segunda generación utilizada para calcular spKt/V, donde ln es el logaritmo natural, R es la relación de urea sérica posdiálisis / prediálisis, t es el tiempo de tratamiento (en horas), UF es el volumen de ultrafiltración (en litros) y W es el peso corporal posdiálisis del paciente (en kilogramos)4,14. Sin embargo, debe tenerse en cuenta que esta ecuación solo es precisa cuando se aplica a la diálisis administrada tres veces por semana durante 2.5-5 horas5.
Kt/V equilibrado (eKt/V)
A diferencia de spKt/V, el Kt/V equilibrado (eKt/V) reconoce que la urea no está confinada a un compartimento del cuerpo. Aunque la concentración de urea en sangre es baja al final de una sesión de diálisis, la urea eventualmente se difundirá fuera de las células y regresará al espacio extracelular. De hecho, el completo equilibrio de la urea entre los compartimentos sanguíneo y tisular no se completa hasta 30-60 minutos después del final de la diálisis4,8. La diferencia entre la concentración de urea en sangre al final de la diálisis y la concentración después del equilibrio total se denomina “rebote de urea”. Dado que los modelos spKt/V no tienen en cuenta este efecto rebote, es probable que sobreestimen la cantidad de diálisis recibida por el paciente8,10,12. Por lo tanto, el eKt/V (a veces llamado Kt/V de doble grupo) se desarrolló para tener en cuenta los efectos del rebote de urea y reflejar con mayor precisión la dosis administrada de diálisis.
Afortunadamente, los pacientes no necesitan permanecer en el centro durante 30 a 60 minutos más mientras se equilibra la urea. El rebote se puede predecir a partir de una concentración sérica de urea posdiálisis no equilibrada y la spKt/V, como se muestra a continuación8,10. Tenga en cuenta que la ecuación cambia dependiendo de si el paciente se dializa mediante un acceso arteriovenoso (p. Ej., Fístula AV) o un acceso estrictamente venoso (p. Ej., Catéter CV).
Acceso arterial: eKt/V=spKt/V- (0.6×spK/V)+0.03
Acceso venoso: eKt/V=spKt/V- (0.47×spK/V)+0.02
Kt/V estándar semanal (stdKt/V)
El interés por una hemodiálisis más frecuente ha llevado a la creación de un Kt/V estándar semanal (stdKt/V) 15. A diferencia de spKt/V y eKt/V, que describen el efecto de una sesión única de tratamiento intermitente, stdKt/V proporciona información sobre el tratamiento para un amplio espectro de terapias dialíticas, incluida la hemodiálisis de frecuencia variable (dos a siete sesiones por semana), continua y diálisis peritoneal intermitente y terapias continuas de reemplazo renal para la insuficiencia renal aguda. Como tal, el modelado cinético de urea con stdKt/V puede ser útil para comparar diferentes regímenes y modalidades de tratamiento4,8,16.
El desarrollo de un stdKt/V fue necesario ya que los cálculos del grupo único y Kt/V equivalente, que se miden tomando las concentraciones de urea antes y después de la diálisis, no reflejan con precisión la dosis de los regímenes de HD más frecuentes. Estos modelos originales son inexactos porque la masa total de urea eliminada por unidad de tiempo disminuye a medida que aumenta el tiempo de tratamiento de diálisis (es decir, no se elimina tanta urea a medida que aumenta la dosis). Por lo tanto, se necesitaba un nuevo modelo, el stdKt/V, para reflejar con precisión la dosis de diálisis que se estaba administrando. Para determinar stdKt/V, el aclaramiento de urea, la generación de urea y la concentración de urea en sangre se calculan durante un período de una semana y se normalizan al agua corporal (o más bien, el volumen total de distribución de urea). Se recomienda un stdKt/V mínimo de 2.0 por semana para todos los pacientes según las pautas de KDOQI y es aproximadamente equivalente a la dosis semanal de tres tratamientos de diálisis únicos con un spKt/V de 1.2 cada uno5. Podemos ver en la Figura 1 que el spKt/V de las sesiones de diálisis por semana no puede simplemente sumarse para determinar la dosis semanal; se debe utilizar una fórmula stdKt/V específica.
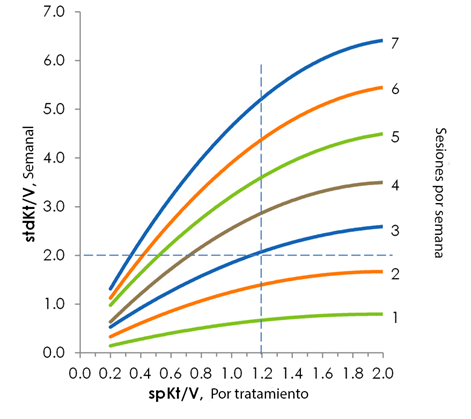 Figura 1. La relación entre spKt/V y stdKt/V no es lineal. Para una duración de sesión estándar de 3.5 horas, puede ver que para lograr un stdKt/V semanal de 2.0, la diálisis tres veces por semana requiere un spKt/V de 1.2. Basado en la referencia 21
Figura 1. La relación entre spKt/V y stdKt/V no es lineal. Para una duración de sesión estándar de 3.5 horas, puede ver que para lograr un stdKt/V semanal de 2.0, la diálisis tres veces por semana requiere un spKt/V de 1.2. Basado en la referencia 21
Relación de reducción de urea (URR)
Debido a la complejidad de UKM, se propuso el índice de reducción de urea (URR) como una alternativa más simple para medir la dosis de diálisis. El URR, que se expresa como porcentaje, se refiere a la reducción en la concentración de urea sérica durante el tratamiento de diálisis y está matemáticamente relacionado con spKt/V, como se muestra a continuación8. En las ecuaciones, Ct y Co representan las concentraciones séricas de urea posdiálisis y prediálisis, respectivamente.
![]()
![]()
El URR se correlaciona bien con los resultados de la diálisis y está reconocido por las pautas de KDOQI como un método aceptable para cuantificar la dosis de diálisis. Sin embargo, a diferencia de la UKM, puede producirse una variabilidad significativa porque la URR no tiene en cuenta la generación de urea intradialítica o la ultrafiltración4,5. Con el fin de proporcionar un aclaramiento adecuado, las pautas de KDOQI recomiendan que los tratamientos de hemodiálisis convencionales tres veces por semana de menos de 5 horas deben tener un URR mínimo del 65% con una dosis objetivo del 70% 5
Impacto del aclaramiento de urea residual (KR)
Estudios previos han demostrado que el aclaramiento de urea residual nativo (KR) de un paciente puede disminuir notablemente la necesidad de diálisis y tener una influencia importante en la mortalidad17. Aunque la magnitud de este aclaramiento es aparentemente pequeña, el KR es un proceso continuo que sirve para atenuar el aumento de toxinas entre tratamientos de diálisis5,10. Muchos nefrólogos en ejercicio no compensan la función residual al calcular la dosis de hemodiálisis debido a la inconveniencia y al costo de las mediciones. Más importante aún, estas prácticas también pueden tener un impacto psicológico negativo, ya que los pacientes verían aumentar continuamente su dosis de diálisis a medida que avanza la enfermedad y se pierde la función renal nativa10. Sin embargo, hay varios métodos disponibles para incorporar KR en el aclaramiento del hemodializador. Estos métodos se analizan en detalle en las pautas más recientes de KDOQI y están más allá del alcance de esta revisión5. A diferencia de la hemodiálisis, las mediciones de la dosis de diálisis peritoneal suelen considerar la FRR como parte de la eliminación adecuada de solutos.
Otros marcadores de dosis de diálisis
Aunque la urea es el marcador más común utilizado para cuantificar la dosis de diálisis, la urea no se correlaciona estrechamente con la eliminación de compuestos solubles en agua más grandes, solutos unidos a proteínas o moléculas intermedias4,6. Como tal, se han investigado otras moléculas como la β2-microglobúmina18, la cistatina-C19 y el fosfato20 como marcadores de la dosis de diálisis.
Referencias
- Locatelli F, Buoncristiani U, Canaud B, Köhler H, Petitclerc T, Zucchelli P. Dialysis dose and frequency. Nephrol Dial Transplant. 2005;20(2):285-296. Available from: http://www.ncbi.nlm.nih.gov/pubmed/15598667.
- Sehgal AR, Leon JB, Siminoff LA, Singer ME, Bunosky LM, Cebul RD. Improving the Quality of Hemodialysis TreatmentA Community-Based Randomized Controlled Trial to Overcome Patient-Specific Barriers. JAMA. 2002;287(15):1961-1967. Available from: https://doi.org/10.1001/jama.287.15.1961.
- Gotch FA. Kt/V is the best dialysis dose parameter. Blood Purif. 2000;18(4):276-285. Available from: http://www.ncbi.nlm.nih.gov/pubmed/10965068.
- Kuhlman MK, Kotanko P, Levin NW, Kuhlmann MK, Kotanko P, Levine NW. Hemodialysis: Outcomes and Adequacy. In: Floege J, Johnson RJ, Feehally J, eds. Comprehensive Clinical Nephrology. 4th ed. Elsevier Saunders; 2010:1060-1068. Available from: http://www.us.elsevierhealth.com/nephrology/comprehensive-clinical-nephrology-expert-consult/9780323058766/.
- KDOQI. Clinical practice guidelines and clinical practice recommendations for 2006 updates: hemodialysis adequacy, peritoneal dialysis adequacy and vascular access. Am J Kidney Dis. 2006;48(48):S1-S322. Available from: http://www.kidney.org/PROFESSIONALS/kdoqi/guideline_upHD_PD_VA/index.htm.
- Depner TA. Uremic toxicity: urea and beyond. Semin Dial. 2001;14(4):246-251. Available from: http://www.ncbi.nlm.nih.gov/pubmed/11489197.
- Gotch F, Sargent J. A mechanistic analysis of the National Cooperative Dialysis Study (NCDS). Kidney Int. 1985;28(3):526-534. Available from: http://www.ncbi.nlm.nih.gov/pubmed/3934452.
- Kotanko P, Levin NW, Gotch FA. Dialysis Delivery and Adequacy. In: Molony DA, Craig JC, eds. Evidenced Based Nephrology. Blackwell Publishing Ltd; 2009:423-430.
- Gotch FA, Sargent JA, Keen ML. Whither goest Kt/V? Kidney Int Suppl. 2000;76:S3-18. Available from: http://www.ncbi.nlm.nih.gov/pubmed/10936795.
- Depner TA. Chapter 6: Approach to Hemodialysis Kinetic Modeling. In: Henrich WL, ed. Principles and Practice of Dialysis. 4th ed. Lippincott Williams & Wilkins; 2009:73-92.
- O’Connor AS, Wish JB. Chapter 8: Hemodialysis Adequacy and the Timing of Dialysis Initiation. In: Henrich WL, ed. Principles and Practice of Dialysis. 4th ed. Lippincott Williams & Wilkins; 2009:106-122.
- Kemp HJ, Parnham A, Tomson CR. Urea kinetic modelling: a measure of dialysis adequacy. Ann Clin Biochem. 2001;38(Pt 1):20-27. Available from: http://www.ncbi.nlm.nih.gov/pubmed/11270837.
- Gotch FA. Evolution of the single-pool urea kinetic model. Semin Dial. 2001;14(4):252-256. Available from: http://www.ncbi.nlm.nih.gov/pubmed/11489198.
- Daugirdas JTT. Second generation logarithmic estimates of single-pool variable volume Kt/V: an analysis of error. J Am Soc Nephrol. 1993;4(5):1205-1213. Available from: http://www.ncbi.nlm.nih.gov/pubmed/8305648.
- Diaz-Buxo JA, Loredo JP. Standard Kt/V: comparison of calculation methods. Artif Organs. 2006;30(3):178-185. Available from: http://www.ncbi.nlm.nih.gov/pubmed/16480392.
- Meyer TW, Sirich TL, Hostetter TH. Dialysis cannot be dosed. Semin Dial. 2011;24(5):471-479. Available from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=4124940&tool=pmcentrez&rendertype=abstract.
- Termorshuizen F, Dekker FFW, van Manen JGJ, et al. Relative contribution of residual renal function and different measures of adequacy to survival in hemodialysis patients: an analysis of the Netherlands Cooperative Study on the Adequacy of Dialysis (NECOSAD)-2. J Am Soc Nephrol. 2004;15(4):1061-1070. Available from: http://www.ncbi.nlm.nih.gov/pubmed/15034110.
- Baurmeister U, Vienken J, Ward R a. Should dialysis modalities be designed to remove specific uremic toxins? Semin Dial. 2009;22(4):454-457. Available from: http://www.ncbi.nlm.nih.gov/pubmed/19709001.
- Huang S-HS, Filler G, Yasin A, Lindsay RM. Cystatin C reduction ratio depends on normalized blood liters processed and fluid removal during hemodialysis. Clin J Am Soc Nephrol. 2011;6(2):319-325. Available from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=3052222&tool=pmcentrez&rendertype=abstract.
- Schmitt CP, Borzych D, Nau B, Wühl E, Zurowska A, Schaefer F. Dialytic phosphate removal: a modifiable measure of dialysis efficacy in automated peritoneal dialysis. Perit Dial Int. 2009;29(4):465-471. Available from: http://www.ncbi.nlm.nih.gov/pubmed/19602613.
- Gotch FA. The current place of urea kinetic modelling with respect to different dialysis modalities. Nephrol Dial Transplant. 1998;13 Suppl 6:10-14. Available from: http://www.ncbi.nlm.nih.gov/pubmed/9719197.
P/N 102476-01S Rev C 02/2023
