Anatomía del Peritoneo
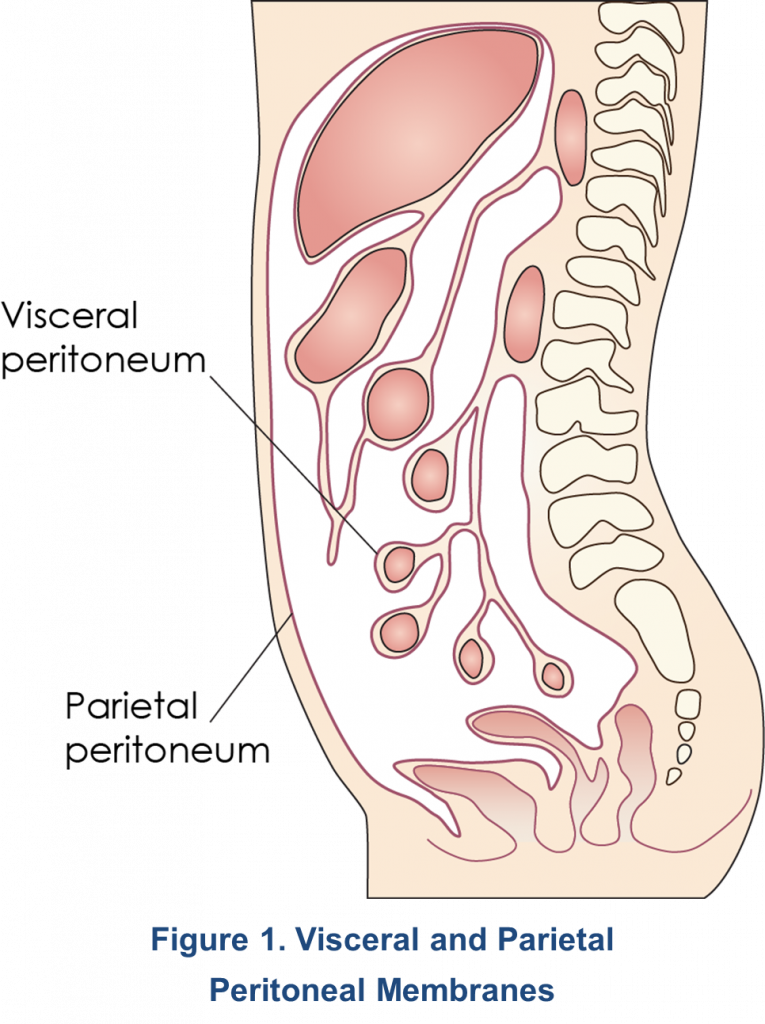 El peritoneo está compuesto por el peritoneo parietal, una membrana heterogénea, serosa y semipermeable que recubre la pared abdominal – y el peritoneo visceral, que recubre los órganos abdominales (Figura 1)1. Su superficie es de aproximadamente 1-2 m2. En los hombres, el peritoneo es un sistema de saco cerrado, mientras que en las mujeres es un sistema de saco abierto con las trompas de Falopio y los ovarios conectados a la cavidad peritoneal. El peritoneo parietal obtiene su irrigación sanguínea de la pared abdominal (regiones lumbares, intercostales y epigástrica) y drena hacia la vena cava inferior, mientras que el peritoneo visceral recibe su irrigación sanguínea de la arteria mesentérica superior y drena hacia la vena porta. El flujo sanguíneo peritoneal total varía de 50 a 150 ml/min2. La cavidad peritoneal, ubicada entre el peritoneo parietal y visceral2, contiene aproximadamente 100 mL de líquido seroso1 y se convierte en el compartimento de dializado durante la diálisis peritoneal (DP), a partir del cual puede ocurrir el intercambio de solutos con la sangre1,3. El drenaje de la cavidad peritoneal lo realiza principalmente el sistema linfático. Es importante destacar que el sistema linfático subdiafragmático es responsable del 70-80% del flujo linfático de la cavidad peritoneal. El sistema linfático también sirve como vía para la eliminación de sustancias extrañas y macromoléculas. En pacientes estables sometidos a DP, la tasa de flujo linfático varía de 7 a 20 ml/h con pérdidas totales de líquido entre 60 a 91 ml/h4.
El peritoneo está compuesto por el peritoneo parietal, una membrana heterogénea, serosa y semipermeable que recubre la pared abdominal – y el peritoneo visceral, que recubre los órganos abdominales (Figura 1)1. Su superficie es de aproximadamente 1-2 m2. En los hombres, el peritoneo es un sistema de saco cerrado, mientras que en las mujeres es un sistema de saco abierto con las trompas de Falopio y los ovarios conectados a la cavidad peritoneal. El peritoneo parietal obtiene su irrigación sanguínea de la pared abdominal (regiones lumbares, intercostales y epigástrica) y drena hacia la vena cava inferior, mientras que el peritoneo visceral recibe su irrigación sanguínea de la arteria mesentérica superior y drena hacia la vena porta. El flujo sanguíneo peritoneal total varía de 50 a 150 ml/min2. La cavidad peritoneal, ubicada entre el peritoneo parietal y visceral2, contiene aproximadamente 100 mL de líquido seroso1 y se convierte en el compartimento de dializado durante la diálisis peritoneal (DP), a partir del cual puede ocurrir el intercambio de solutos con la sangre1,3. El drenaje de la cavidad peritoneal lo realiza principalmente el sistema linfático. Es importante destacar que el sistema linfático subdiafragmático es responsable del 70-80% del flujo linfático de la cavidad peritoneal. El sistema linfático también sirve como vía para la eliminación de sustancias extrañas y macromoléculas. En pacientes estables sometidos a DP, la tasa de flujo linfático varía de 7 a 20 ml/h con pérdidas totales de líquido entre 60 a 91 ml/h4.
Seis Capas del Peritone
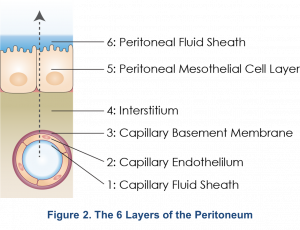
La membrana peritoneal está compuesta por seis capas que consisten en la película de líquido capilar, el endotelio capilar, la membrana basal endotelial, el intersticio, el mesotelio y la película de fluido (Figura 2)1. Anteriormente se pensaba que las seis capas proporcionaban diferentes niveles de resistencia a los solutos, y la capa mesotelial con su gran superficie funcionaba como dializador. Sin embargo, el modelo de tres poros (abajo) sugiere que el capilar peritoneal
es la barrera crítica para el transporte peritoneal5.
El modelo de tres poros
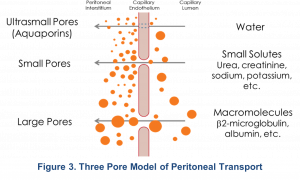
El modelo de tres poros (MTP) del peritoneo define el transporte de agua y solutos a través del capilar peritoneal por medio de poros de tres tamaños diferentes: poros grandes, pequeños y ultrapequeños5. Este modelo ha sido validado por observaciones clínicas5,6. Los poros grandes varían de 10 a 20 nm (100 a 250 A°) de tamaño y están formados por hendiduras entre las células endoteliales. Los poros grandes son pequeños en número, <0.01% del total de poros y representan <10% de la remoción de solutos (macromoléculas). Los poros pequeños son más numerosos, también están formados por hendiduras entre las células endoteliales, representan >90% de la eliminación de solutos (solutos pequeños) y agua, y tienen un diámetro de 4-6 nm. Los poros ultrapequeños, compuestos principalmente de Acuaporina-1, varían en tamaño de 0,4 a 0,6 nm y son canales transcelulares en las células endoteliales que transportan agua únicamente y proporcionan un 0% de eliminación de solutos5. El transporte de agua a través de la Acuaporina-1 también se conoce como “transporte de agua libre” y contribuye a ~50% de la ultrafiltración en DP5.
Aunque este modelo sugiere que el intersticio también puede contribuir a la resistencia al transporte de solutos, no hay resistencia del mesotelio en sí ni de las capas de líquido estancadas. Investigación adicional se ha ampliado sobre este modelo. Ronco propuso que la vasculatura peritoneal, en particular el área de superficie de los capilares peritoneales, en lugar de toda la superficie del peritoneo y el intersticio, es responsable de facilitar el transporte de solutos8. Específicamente, la distancia de cada capilar peritoneal al mesotelio determina la contribución relativa de ese capilar al área de superficie efectiva y las propiedades de resistencia de la membrana. Este concepto se denomina “hipótesis del capilar más cercano”, donde los capilares más cercanos al mesotelio experimentan un mayor efecto osmótico en comparación con los más alejados. Dado que los pacientes con la misma área de superficie peritoneal total pueden tener grados muy diferentes de vascularización peritoneal, sus áreas de superficie peritoneal efectivas también variarían ampliamente. Además, en un solo paciente, la superficie peritoneal puede verse alterada por eventos específicos como episodios de peritonitis9.
Fisiología del transporte peritoneal
Mecanismos de transporte
El transporte peritoneal de solutos y agua depende de cuatro mecanismos que ocurren simultáneamente: difusión, ósmosis, convección y absorción de fluidos1,10.
Transporte de electrolitos y solutos
Difusión
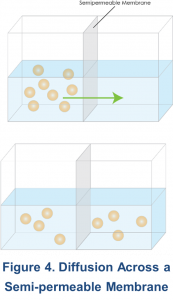 El proceso de difusión da como resultado el movimiento neto de moléculas de soluto desde un área donde están en alta concentración a un área donde su concentración es baja, a través de una membrana semipermeable (Figura 4). Aunque el soluto se mueve aleatoriamente en ambas direcciones, hay más soluto moviéndose de una concentración alta a una baja que en la dirección opuesta. Eventualmente, las concentraciones se vuelven iguales en ambos lados de la membrana y el movimiento neto en cada dirección es cero. Un concepto importante es que el movimiento de las moléculas de soluto es aleatorio y está impulsado por energía térmica que aumenta proporcionalmente cuanto mayor es la temperatura por encima del cero absoluto (–273 grados centígrados). Esta energía térmica se transforma en energía cinética, que es el producto de la masa y la velocidad. Dado que esta energía es la misma para moléculas de diferentes tamaños a la misma temperatura, las moléculas más grandes tienden a moverse más lentamente que las más pequeñas11. Además del gradiente de concentración, la difusión peritoneal depende del área de superficie peritoneal disponible para el transporte, la resistencia intrínseca de la membrana y el peso molecular del soluto a transportar10.
El proceso de difusión da como resultado el movimiento neto de moléculas de soluto desde un área donde están en alta concentración a un área donde su concentración es baja, a través de una membrana semipermeable (Figura 4). Aunque el soluto se mueve aleatoriamente en ambas direcciones, hay más soluto moviéndose de una concentración alta a una baja que en la dirección opuesta. Eventualmente, las concentraciones se vuelven iguales en ambos lados de la membrana y el movimiento neto en cada dirección es cero. Un concepto importante es que el movimiento de las moléculas de soluto es aleatorio y está impulsado por energía térmica que aumenta proporcionalmente cuanto mayor es la temperatura por encima del cero absoluto (–273 grados centígrados). Esta energía térmica se transforma en energía cinética, que es el producto de la masa y la velocidad. Dado que esta energía es la misma para moléculas de diferentes tamaños a la misma temperatura, las moléculas más grandes tienden a moverse más lentamente que las más pequeñas11. Además del gradiente de concentración, la difusión peritoneal depende del área de superficie peritoneal disponible para el transporte, la resistencia intrínseca de la membrana y el peso molecular del soluto a transportar10.
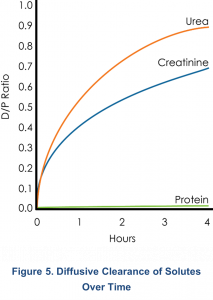 La difusión es por lejos, el proceso más importante involucrado en el transporte de electrolitos y solutos en la diálisis peritoneal (DP). Ejemplos de tales solutos incluyen: urea, creatinina, K+, H+, HCO3–, fosfato, albúmina, proteínas y toxinas3,7. El transporte difusivo de Na+ y Ca2+ es mínimo10.
La difusión es por lejos, el proceso más importante involucrado en el transporte de electrolitos y solutos en la diálisis peritoneal (DP). Ejemplos de tales solutos incluyen: urea, creatinina, K+, H+, HCO3–, fosfato, albúmina, proteínas y toxinas3,7. El transporte difusivo de Na+ y Ca2+ es mínimo10.
El flujo de difusión es más alto en la primera hora y disminuye con el tiempo. Por ejemplo, como se muestra en la Figura 1, la urea se equilibra >90% en 4 horas y la creatinina se equilibra >60%. El transporte adicional de solutos pequeños es mínimo y las estancias prolongadas son más importantes para la eliminación de solutos de mayor peso molecular (PM), como la microglobulina β-2 y la albúmina9.
Convección
En el transporte de convección, el disolvente (es decir, el agua) transporta los solutos disueltos a través de todos los poros de la membrana, excepto las Acuaporinas-1. Esto es más pronunciado si se utilizan concentraciones más altas de agentes osmóticos en el dializado1.
Transporte de Agua
Ósmosis y Ultrafiltración
La ósmosis se puede definir como el movimiento de un disolvente (es decir, agua) desde un área de baja concentración de soluto a un área de mayor concentración de soluto a través de una membrana semipermeable3. En el transporte peritoneal, el movimiento del agua ocurre igualmente a través de los poros pequeños y las Acuaporinas-1, como se describe en el modelo de tres poros5.
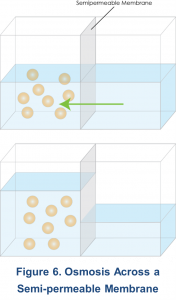 La ultrafiltración (UF) es el proceso que ocurre como resultado del gradiente osmótico (es decir, presión osmótica) creado entre la solución de diálisis relativamente hipertónica y la sangre capilar peritoneal relativamente hipotónica. Con el uso de soluciones de diálisis hipertónica, la ultrafiltración puede conducir a la eliminación de líquidos y a la eliminación por convección de solutos, especialmente moléculas de tamaño mediano. Sin embargo, la eficacia de la ultrafiltración puede verse afectada por varios factores. Estos incluyen la conductancia hidráulica de la membrana peritoneal, el coeficiente de reflexión para el agente osmótico, el agente osmótico utilizado, la concentración y gradiente osmótico, el área de superficie peritoneal efectiva, el tiempo de permanencia y el gradiente de presión hidrostática, que se discuten con más detalle más adelante.
La ultrafiltración (UF) es el proceso que ocurre como resultado del gradiente osmótico (es decir, presión osmótica) creado entre la solución de diálisis relativamente hipertónica y la sangre capilar peritoneal relativamente hipotónica. Con el uso de soluciones de diálisis hipertónica, la ultrafiltración puede conducir a la eliminación de líquidos y a la eliminación por convección de solutos, especialmente moléculas de tamaño mediano. Sin embargo, la eficacia de la ultrafiltración puede verse afectada por varios factores. Estos incluyen la conductancia hidráulica de la membrana peritoneal, el coeficiente de reflexión para el agente osmótico, el agente osmótico utilizado, la concentración y gradiente osmótico, el área de superficie peritoneal efectiva, el tiempo de permanencia y el gradiente de presión hidrostática, que se discuten con más detalle más adelante.
- Conductancia hidráulica de la membrana peritoneal3: Refleja la densidad de los poros pequeños y ultrapequeños en los capilares peritoneales y la distribución de las distancias de los capilares al mesotelio. Difiere entre pacientes.
- Coeficiente de reflexión para el agente osmótico3: Con un rango de 0 y 1, el coeficiente de reflexión refleja la efectividad del agente osmótico para difundirse fuera de la solución de diálisis hacia los capilares peritoneales. Los valores más bajos indican que el agente osmótico se difundirá fuera de la solución de diálisis al cuerpo del paciente a velocidades más rápidas, lo que conducirá a una ultrafiltración menos sostenida. El coeficiente de reflexión de la glucosa es de aproximadamente 0,3, mientras que las formulaciones de poliglucosa más nuevas tienen valores cercanos a 13.
- Agente osmótico utilizado / concentración y gradiente osmótico1: Se utilizan habitualmente dextrosa en concentraciones de 1,5%, 2,5% y 4,25% (1,36%, 2,27% y 3,86% dextrosa anhidra, respectivamente). Otros agentes osmóticos en la DP incluyen 7,5% de poliglucosa (icodextrina) y 1,1% de aminoácidos. La concentración osmótica del dializado en relación con la sangre determina hasta qué punto se intercambian fluidos entre la solución de DP y la sangre. Una alta concentración osmótica en el dializado crea un alto gradiente. La dextrosa se absorbe continuamente durante la diálisis, lo que reduce el gradiente osmótico y conduce a una disminución de la ultrafiltración con el tiempo de permanencia. La icodextrina se absorbe a un ritmo más lento que la glucosa, lo que permite una ultrafiltración sostenida. Las soluciones de PD de aminoácidos al 1,1% son similares, con respecto a UF, a las soluciones de dextrosa al 1,5%12.
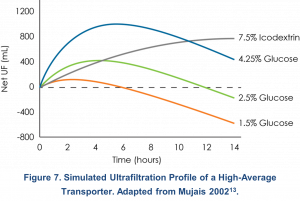 La Figura 2 muestra una simulación por computadora de la ultrafiltración neta obtenida con el uso de soluciones de DP de varias concentraciones de dextrosa y con icodextrina durante un período de 14 horas en un transportador de promedio alto13. Según esta simulación, una sola permanencia de 12 horas con icodextrina al 7,5% proporciona alrededor de 600 ml de UF. La glucosa es más apropiada si se usa para tiempos de permanencia más cortos. Con una sola permanencia de 4 horas de dextrosa al 2.5%, se estima alrededor de 400 ml de UF.
La Figura 2 muestra una simulación por computadora de la ultrafiltración neta obtenida con el uso de soluciones de DP de varias concentraciones de dextrosa y con icodextrina durante un período de 14 horas en un transportador de promedio alto13. Según esta simulación, una sola permanencia de 12 horas con icodextrina al 7,5% proporciona alrededor de 600 ml de UF. La glucosa es más apropiada si se usa para tiempos de permanencia más cortos. Con una sola permanencia de 4 horas de dextrosa al 2.5%, se estima alrededor de 400 ml de UF.
- Área de superficie peritoneal efectiva1: El área de superficie peritoneal efectiva está determinada por el área de la membrana en contacto directo con el dializado y el número de capilares peritoneales perfundidos, que varía ampliamente de un paciente a otro.
- Tiempo de permanencia: para las soluciones a base de glucosa, el gradiente osmótico disminuye durante el transcurso de una permanencia y la velocidad depende del tipo de transporte del paciente. El equilibrio de glucosa entre la solución de DP y el plasma se alcanza más rápido para los transportadores altos y más lento para los transportadores bajos1. Por esta razón, el tiempo de permanencia debe personalizarse según el tipo de transporte del paciente. Generalmente, el pico de UF con soluciones a base de glucosa ocurre entre 2 y 5 horas para transportadores altos y entre 4 y 8 horas para transportadores bajos13. La UF con 7,5% de icodextrina seguirá aumentando a un ritmo lento durante periodos de tiempo mucho más prolongados13.
- Gradiente de presión hidrostática1: la presión hidrostática en un capilar peritoneal es generalmente alrededor de 20 mmHg, que es más alta que la presión intraperitoneal (7 mmHg). Esta diferencia de presión favorece la eliminación de líquidos. Durante la terapia de DP, los aumentos en la presión intraperitoneal desde el dializado o la posición del cuerpo, por ejemplo, reducen el gradiente de presión hidrostática y podrían reducir la ultrafiltración.
Tamizado
El tamizado es un mecanismo de transporte en el que un soluto que normalmente se movería con agua a través de una membrana semipermeable por convección es retenido o “tamizado”. Cada soluto tiene un coeficiente de tamizado que depende de su peso molecular y carga. El coeficiente de cribado de un soluto también puede variar entre pacientes debido a variaciones en la distribución de los poros en el endotelio capilar1. Como se mencionó anteriormente, alrededor del 50% de la ultrafiltración ocurre en los poros ultra pequeños, específicamente a través de Aquaporin-15. El transporte a través de los poros ultra pequeños es “transporte de agua libre”, lo que significa que el agua está libre de todos los solutos. En otras palabras, todos los solutos se tamizan en los poros ultra pequeños. Como resultado, los solutos como el sodio no se mueven a través de la membrana en la misma proporción que el agua; esto puede provocar la acumulación de sodio en el cuerpo. Este efecto se llama tamizado de sodio. El tamizado de sodio se produce durante la fase inicial de la permanencia en la EP y es más pronunciado con las soluciones de EP con mayor contenido de glucosa. En el caso del sodio, el tamizado es especialmente relevante ya que las soluciones de DP generalmente tienen una concentración de sodio casi fisiológica que no crea un gradiente de difusión suficiente para una eliminación eficaz del sodio1.
Absorcion de fluidos1
El agua y los solutos del dializado son absorbidos por el sistema linfático a una velocidad relativamente constante de 1 a 2 ml / min. La absorción constante de líquidos durante la DP limita la duración de una permanencia en la DP, ya que el líquido de la cavidad peritoneal se transportará al cuerpo del paciente. La absorción de líquido linfático varía entre individuos, pero las razones no se comprenden bien.
References:
- Blake PG, Daugirdas JT. Physiology of Peritoneal Dialysis. In: Daugirdas JT, Blake PG, Ing TS, eds. Handbook of Dialysis. 5th ed. Walters Kluwer Health; 2015:392-407.
- Gotloib L. Functional Structure of the Peritoneum as a Dialyzing Membrane. In: Khanna R, Krediet RT, eds. Textbook of Peritoneal Dialysis. 3rd ed. Springer US; 2009:73-135.
- Flessner MF. Peritoneal transport physiology: insights from basic research. J Am Soc Nephrol. 1991;2(2):122-135. Available from: http://www.ncbi.nlm.nih.gov/pubmed/1954325.
- Flessner MF. Solute and water transport across the peritoneal membrane. In: Ronco C, Bellomo R, Kellum JA, eds. Critical Care Nephrology. 2nd ed. Saunders Elsevier; 2009:1472-1478.
- Devuyst O, Rippe B. Water transport across the peritoneal membrane. Kidney Int. 2014;85(4):750-758. Available from: http://www.ncbi.nlm.nih.gov/pubmed/23802191.
- Rippe B, Stelin G. Simulations of peritoneal solute transport during CAPD. Application of two-pore formalism. Kidney Int. 1989;35(5):1234-1244. Available from: http://www.ncbi.nlm.nih.gov/pubmed/2770105.
- Rippe B, Stelin G, Haraldsson B. Computer simulations of peritoneal fluid transport in CAPD. Kidney Int. 1991;40(2):315-325. Available from: http://www.ncbi.nlm.nih.gov/pubmed/1942781.
- Ronco C. The “nearest capillary” hypothesis: a novel approach to peritoneal transport physiology. Perit Dial Int. 1996;16(2):121-125. Available from: http://www.ncbi.nlm.nih.gov/pubmed/9147543.
- Holmes CJ. Abnormalities of Host Defense Mechanisms During Peritoneal Dialysis. In: Nissenson AR, Fine RN, eds. Dialysis Therapy. 3rd ed. Hanley & Belfus; 2002:235-238.
- Krediet RT. The Physiology of Peritoneal Solute, Water, and Lymphatic Transport. In: Khanna R, Krediet R, eds. Textbook of Peritoneal Dialysis. 3rd ed. Springer Science+Business Media; 2009:137-172.
- Fowler S, Roush R, Wise J. Cell Struture and Function. In: Concepts of Biology. OpenStax; 2013.
- Shockley TR, Martis L, Tranaeus AP. New solutions for peritoneal dialysis in adult and pediatric patients. Perit Dial Int. 1999;19 Suppl 2:S429-34. Available from: http://www.ncbi.nlm.nih.gov/pubmed/10406559.
- Mujais S, Vonesh EEF. Profiling of peritoneal ultrafiltration. Kidney Int Suppl. 2002;62(81):S17-S22. Available from: https://www.ncbi.nlm.nih.gov/pubmed/12230478.
P/N 102479-01S Rev B 02/2023
