Protección Endotelial y Aterosclerosis
La mortalidad cardiovascular en pacientes en diálisis es 10-20 veces mayor que en la población general y parece ser más de 100 veces mayor en pacientes menores de 45 años (1). La etiología de la enfermedad cardiovascular en pacientes con enfermedad renal en etapa terminal ERET es compleja y multifactorial; La sobrecarga de volumen y presión, las anomalías en la morfología y función cardíacas, las dislipidemias, la aterosclerosis y los trastornos nutricionales, todos influyen.
En el corazón de la aterosclerosis hay un endotelio anormal y disfuncional. Las células progenitoras endoteliales derivadas de la médula ósea (CPE) son importantes para el mantenimiento del endotelio. Las CPE median la reparación del endotelio vascular dañado, promueven la angiogénesis y protegen el vaso sanguíneo del desarrollo de la aterosclerosis (2). Varios informes en la literatura describen anomalías cualitativas y cuantitativas de las CPE en pacientes urémicos y dializados (3-7).
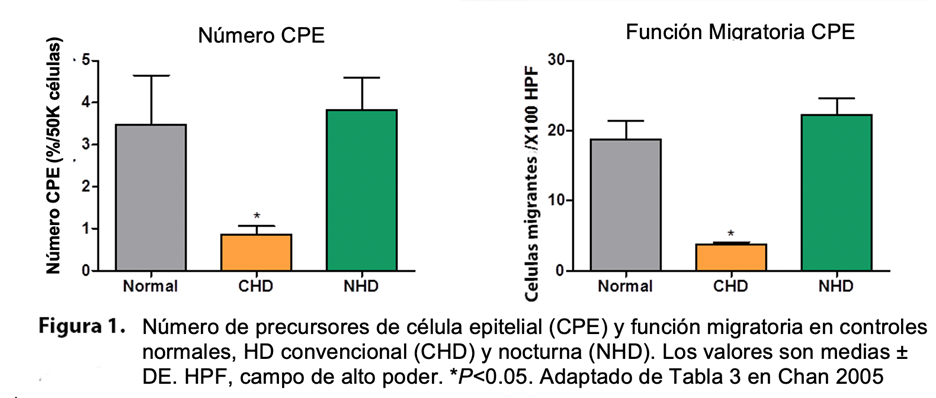
La intensificación de la prescripción de hemodiálisis no tiene un efecto directo sobre el número de células progenitoras endoteliales; sin embargo, Chan et al. planteó la hipótesis de que la eliminación mejorada de la toxina urémica durante la hemodiálisis nocturna diaria puede resultar en una mejora en el número y la función de CPE, mejorando los parámetros cardiovasculares generales en los pacientes en diálisis. Las CPE se aislaron de 3 grupos de sujetos de la misma edad y sexo (control normal, n = 10; HD convencional, tres veces por semana (CHD), n = 12; y HD diaria, nocturna, n = 10 pacientes) (8). Ninguno de los pacientes presentaba enfermedad cardiovascular sintomática. La función de CPE se evaluó mediante pruebas in vitro de la respuesta migratoria a 50 ng / ml de factor de crecimiento endotelial vascular. El índice de masa del ventrículo izquierdo (IMVI) se obtuvo mediante ecocardiografía 2D. El número y la función de CPE se vieron notablemente afectados en pacientes con cardiopatía coronaria a pesar de las dosis más altas de eritropoyetina. Por el contrario, los pacientes con NHD tenían una biología de CPE similar a los controles normales (Figura 1). El número y la función de CPE se correlacionan inversamente con la concentración de urea previa a la diálisis y el IMVI.
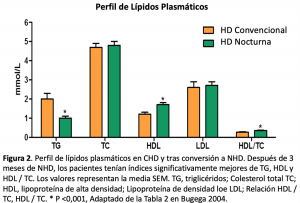
Además de los parámetros de CPE, varios artículos han descrito una mejoría de la dislipidemia con hemodiálisis intensificada. Dado que esto tampoco podría ser un efecto directo, se supone que la HD intensificada elimina mejor uno o más solutos que deterioran el metabolismo lipídico normal. Bugeja y cols. realizó un estudio de cohorte prospectivo de 11 pacientes con ERT antes y después de la conversión de hemodiálisis convencional a diaria (5-6 veces / semana) nocturna (9). Se obtuvo un perfil de lípidos en ayunas de 12 horas mientras estaba en CHD y después de 3 meses en NHD estable. Tres meses después de la conversión de CHD a NHD, se identificó una caída significativa en los triglicéridos séricos asociada con un aumento significativo en el colesterol HDL y la relación HDL/colesterol total como se muestra en la Figura 2. El colesterol total y el colesterol LDL permanecieron sin cambios. Aunque los cambios de esta magnitud en el perfil de lípidos podrían considerarse como una respuesta clínicamente significativa a cualquier otro tratamiento hipolipemiante, debe tenerse en cuenta que los ensayos controlados aleatorios con fármacos hipolipemiantes (estatinas) no han mostrado ninguna mejora en los resultados clínicos en pacientes en mantenimiento. HD (10-11).
Referencias:
- Foley RN, Parfrey PS, Sarnak MJ. Epidemiology of cardiovascular disease in chronic renal disease. J Am Soc Nephrol. 1998;9(12 Suppl):S16-23. Available from: http://www.ncbi.nlm.nih.gov/pubmed/11443763.
- Hill JM, Zalos G, Halcox JPJ, Schenke WH, Waclawiw MA, Quyyumi AA, Finkel T. Circulating endothelial progenitor cells, vascular function, and cardiovascular risk. N Engl J Med. 2003;348(7):593-600. Available from: http://www.ncbi.nlm.nih.gov/pubmed/12584367.
- Bahlmann FH, DeGroot K, Duckert T, Niemczyk E, Bahlmann E, Boehm SM, Haller H, Fliser D. Endothelial progenitor cell proliferation and differentiation is regulated by erythropoietin. Kidney Int. 2003;64(5):1648-1652. Available from: http://www.ncbi.nlm.nih.gov/pubmed/14531796.
- Chen Y-LY-T, Cheng B-C, Ko S-F, Chen C-H, Tsai T-H, Leu S, Chang H-W, Chung S-Y, Chua S, Yeh K-H, et al. Value and level of circulating endothelial progenitor cells, angiogenesis factors and mononuclear cell apoptosis in patients with chronic kidney disease. Clin Exp Nephrol. 2013;17(1):83-91. Available from: http://www.ncbi.nlm.nih.gov/pubmed/22814956.
- Jourde-Chiche N, Dou L, Sabatier F, Calaf R, Cerini C, Robert S, Camoin-Jau L, Charpiot P, Argiles A, Dignat-George F, et al. Levels of circulating endothelial progenitor cells are related to uremic toxins and vascular injury in hemodialysis patients. J Thromb Haemost. 2009;7(9):1576-1584. Available from: http://www.ncbi.nlm.nih.gov/pubmed/19583820.
- Krieter DH, Fischer R, Merget K, Lemke H-D, Morgenroth A, Canaud B, Wanner C. Endothelial progenitor cells in patients on extracorporeal maintenance dialysis therapy. Nephrol Dial Transplant. 2010;25(12):4023-4031.
- Kun-Ying Z, Hui-Lan L, Xiao-Feng D, Guo-Gang L. Association between Circulating Endothelial Cells and Carotid Atherosclerosis in Patients Receiving Maintenance Hemodialysis. 2014. Available from: http://dx.doi.org/10.1155/2014/753759.
- Chan CT, Li SH, Verma S. Nocturnal hemodialysis is associated with restoration of impaired endothelial progenitor cell biology in end-stage renal disease. Am J Physiol Renal Physiol. 2005;289(4):F679-84. Available from: http://www.ncbi.nlm.nih.gov/pubmed/15928211.
- Bugeja AL, Chan CT. Improvement in lipid profile by nocturnal hemodialysis in patients with end-stage renal disease. ASAIO J. 2004;50(4):328-331. Available from: http://www.ncbi.nlm.nih.gov/pubmed/15307542.
- Wanner C, Krane V, März W, Olschewski M, Mann JFE, Ruf G, Ritz E. Atorvastatin in patients with type 2 diabetes mellitus undergoing hemodialysis. N Engl J Med. 2005;353(3):238-248. Available from: http://www.ncbi.nlm.nih.gov/pubmed/16034009.
- Fellström BC, Jardine AG, Schmieder RE, Holdaas H, Bannister K, Beutler J, Chae D-W, Chevaile A, Cobbe SM, Grönhagen-Riska C, et al. Rosuvastatin and cardiovascular events in patients undergoing hemodialysis. N Engl J Med. 2009;360(14):1395-1407. Available from: http://www.ncbi.nlm.nih.gov/pubmed/19332456.
P/N 102559-01S Rev B 02/2023